Home Seltene Krankheiten Stoffwechselerkrankungen
Stoffwechselerkrankungen: Vielfältige Störungen des menschlichen Metabolismus
Denkt man an Stoffwechselkrankheiten, kommen einem vermutlich als Erstes häufige Erkrankungen wie Diabetes mellitus oder Funktionsstörungen der Schilddrüse in den Sinn. Tatsächlich gibt es aber allein mehr als 500 verschiedene Krankheiten, die auf angeborenen Störungen des Stoffwechsels beruhen.
In diesem Beitrag möchten wir einen Überblick geben, wie unser Stoffwechsel funktioniert und wie es zu Stoffwechselstörungen kommt sowie einige seltene Stoffwechselerkrankungen vorstellen:
Metabolismus: Der menschliche Stoffwechsel
Stoffwechselprozesse: Verschiedene Wege der Nährstoffverwertung
Störungen des Stoffwechsels: Entstehung diverser Erkrankungen
Gendefekte: Ursache angeborener Stoffwechselkrankheiten
Seltene angeborene Stoffwechselerkrankungen: LAL-D, HPP, AL-Amyloidose und Morbus Wilson
Diagnose: Stoffwechselerkrankungen erkennen
Behandlung: Zielgerichtete Therapieansätze
Metabolismus: Der menschliche Stoffwechsel
Der Mensch besteht aus rund 30 Billionen Zellen. Jede einzelne davon benötigt eine Versorgung mit Nährstoffen und einen Abtransport von Abfallstoffen. Für die Bildung, Unterhaltung und Regeneration von Geweben sind zudem spezielle Baustoffe notwendig, die den Zellen zur Verfügung stehen müssen. Innerhalb der Zellen laufen Stoffwechselprozesse zur Gewinnung von Energie, zum Aufbau von Eiweißen, zum Abbau von Abfallstoffen, zum Erhalt der Zelle und zur Erfüllung weiterer Funktionen ab, wie z. B. der Speicherung von Fett als Energiereserve.
Die Gesamtheit all dieser Vorgänge im Körper wird unter dem Begriff Stoffwechsel oder auch Metabolismus zusammengefasst.
Stoffwechselprozesse: Verschiedene Wege der Nährstoffverwertung
Das „Zentrallabor“ des menschlichen Körpers ist die Leber. Sie nimmt eine wichtige Rolle bei zahlreichen Stoffwechselprozessen ein. Alle Stoffe, die durch den Darm resorbiert und in die Blutbahn aufgenommen werden, gelangen zunächst in die Leber. Dort werden sie weiterverarbeitet und umgewandelt, direkt verwertet oder gespeichert und teilweise sofort wieder abgebaut und über die Galle ausgeschieden oder nierengängig gemacht, so dass sie über die Niere ausgeschieden werden können.
Für den Kohlenhydratstoffwechsel zur Energiegewinnung spielt die Glukose (Traubenzucker) eine bedeutende Rolle. Wird diese von den Körperzellen benötigt, kann die Leber Glukose in die Blutbahn abgeben. Andernfalls kann die Glukose in Form von Glykogen in den Leberzellen zur kurzfristigen Speicherung eingelagert werden oder als langfristige Energiereserve in Fett umgewandelt werden. Für die Steuerung des Blutzuckerspiegels sind Hormone der Bauchspeicheldrüse zuständig, die unter anderem die Aufnahme von Glukose in den peripheren Zellen regulieren. In den Körperzellen wird die Glukose als Energielieferant benötigt. Dort wird die Glukose durch die sogenannte Glykolyse in einer vielstufigen Reaktionskette abgebaut und Energie gewonnen. Hierbei entsteht CO 2 als Abbauprodukt, das über die Blutbahn abtransportiert und über die Lunge ausgeatmet wird.
Eine Energiegewinnung ist in den Zellen auch aus anderen Substanzen, wie z. B. Fetten möglich. Der Fettstoffwechsel regelt den Aufbau, Umbau und Abbau von Lipiden. Fette werden über die Nahrung aufgenommen und vom Darm resorbiert, können aber auch von Körperzellen synthetisiert werden. Im Blut werden die Fette durch Lipoproteine als Transportvehikel zu ihrem Ziel, z. B. den Muskelzellen oder Fettzellen transportiert. Werden die Lipide nicht direkt weiterverwertet, können sie im Fettgewebe als Energiespeicher für „schlechte Zeiten“ eingelagert werden. Lipide sind jedoch nicht nur für die Energiegewinnung wichtig. Sie sind auch ein essenzieller Baustein der Zellmembran und werden für die Synthese von zahlreichen Hormonen benötigt.
Für den Aufbau von Geweben und Strukturen benötigt der menschliche Körper Proteine. Die Zufuhr der für den Eiweißstoffwechsel notwendigen Aminosäuren erfolgt in der Form von Eiweiß über die Nahrung. Im Darm werden die komplexen Eiweiße zu einfachen Aminosäuren zerlegt, im Dünndarm resorbiert und dann im Blut zur Leber und zum gesamten Körper transportiert. Der Aufbau von neuen Proteinen aus Aminosäuren wird Proteinsynthese genannt und findet in allen Zellen statt. Die Leberzellen spielen bei der Synthese von Enzymen und Hormonen eine wichtige Rolle. Proteine können auch als Energiequelle eingesetzt, von den Zellen abgebaut und in den Energiestoffwechsel eingeschleust werden.
Neben den klassischen Wegen des Glukose-, Fett- und Eiweißstoffwechsels besitzt der Mensch zahlreiche weitere Stoffwechselwege, die für den Aufbau und Erhalt des Körpers notwendig sind.
Ein Beispiel ist der Knochenstoffwechsel, der den Auf- und Abbau von Knochensubstanz regelt und die Versorgung der Knochenzellen sicherstellt. Auch wenn die Knochen von außen betrachtet sehr statisch wirken, so findet dort ständig ein Knochenaufbau durch Osteoblasten und ein Knochenabbau durch Osteoklasten statt. Nur wenn sich diese beiden Prozesse im Gleichgewicht befinden und die Mineralstoffe Kalzium und Phosphat in ausreichendem Maße vorhanden sind, können sich stabile Knochen bilden. Gesteuert wird der Knochenstoffwechsel von mehreren Hormonen, unter anderem den Geschlechtshormonen und einem Hormon der Hirnanhangsdrüse (Hypophyse).
Störungen des Stoffwechsels: Entstehung diverser Erkrankungen
Der menschliche Stoffwechsel wird durch ein komplexes und ineinandergreifendes System an Hormonen und Enzymen gesteuert. Selbst ein relativ einfach erscheinender Prozess, wie z. B. der Abbau der Glukose durch die Glykolyse, stellt in Wirklichkeit schon eine zehnstufige Reaktionskette dar. An jedem einzelnen Reaktionsschritt ist ein anderes Enzym beteiligt. Nur wenn alle Enzyme in ausreichender Menge vorliegen, kann die Reaktionskette komplett ablaufen. Bereits der Mangel eines Enzyms oder eines Hormons kann zu einer folgenschweren Stoffwechselstörung führen. Die Auswirkungen sind mannigfaltig: Es entsteht ein Mangel an gewünschten Endprodukten. Gleichzeitig kommt es zu einer Ansammlung von nicht ab- bzw. umgebauten Stoffwechselprodukten.
Da die Anzahl an Enzymen und Hormonen, die die Stoffwechselreaktionen fein ausbalanciert steuern, sehr groß ist, existieren entsprechend viele Störungsmöglichkeiten. Das erklärt, warum über 500 verschiedene Stoffwechselerkrankungen bekannt sind, die zum Teil zu den seltenen Erkrankungen zählen, da sie nur wenige Menschen betreffen. In der Summe ist jedoch eine beträchtliche Anzahl an Patienten von diesen seltenen Erkrankungen betroffen.
Gendefekte: Ursache angeborener Stoffwechselkrankheiten
Stoffwechselerkrankungen können erworben oder angeboren sein. Insbesondere die seltenen Stoffwechselerkrankungen sind zumeist angeboren. Durch einen Gendefekt wird ein nicht funktionsfähiges Enzym oder zu wenig von einem Enzym oder Hormon gebildet. Diese Gendefekte entstehen durch spontane Mutation oder Vererbung.
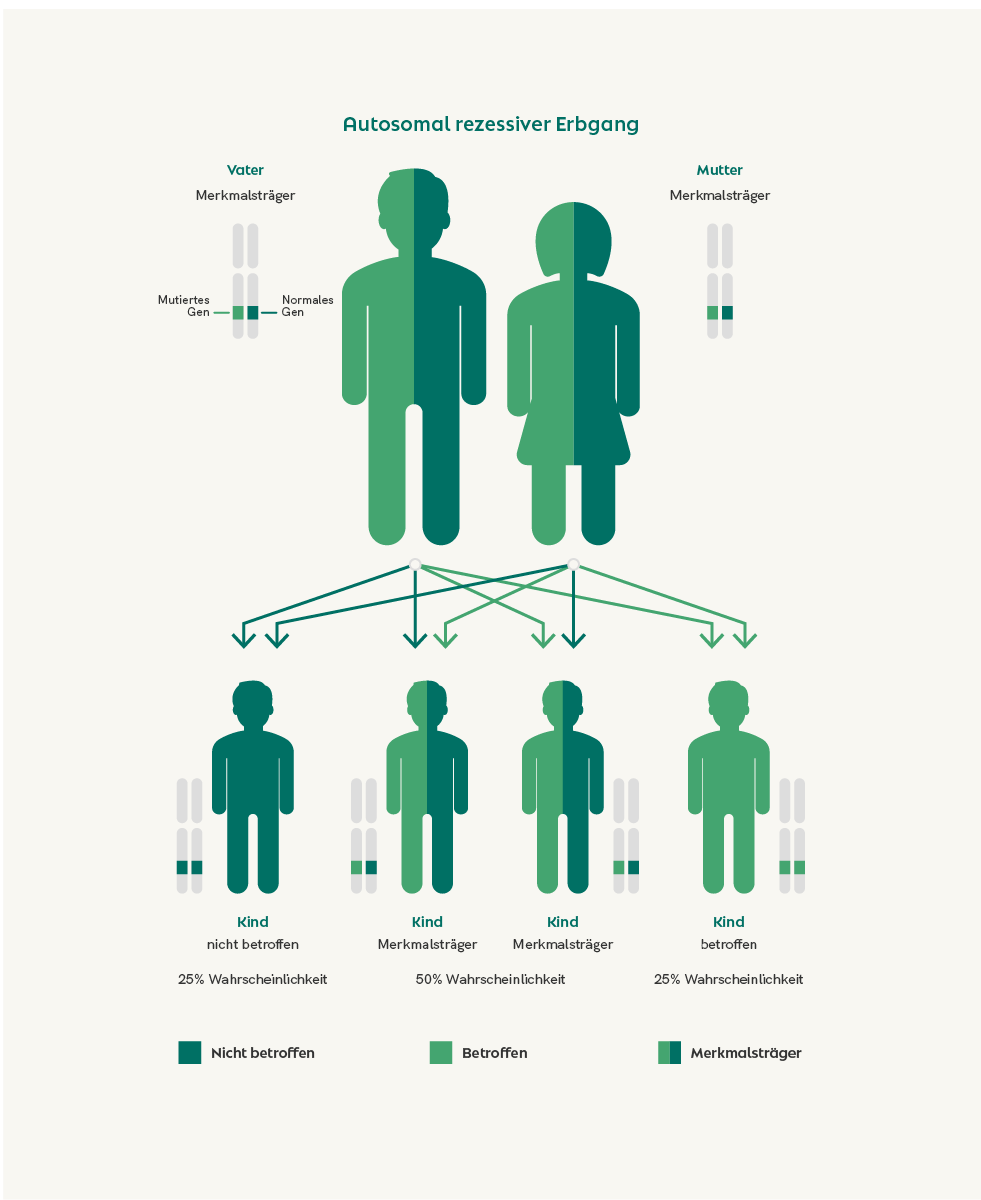
Der häufigste Vererbungsmodus ist die autosomal-rezessive Vererbung (siehe nebenstehende Grafik), sie macht rund 80% der Fälle aus. Symptome treten auf, wenn auf beiden Chromosomen der Gendefekt vorhanden ist. Das Kind bekommt in diesem Fall von jedem Elternteil den Gendefekt vererbt, auch wenn die Eltern selbst nicht erkrankt sind, da sie den Defekt in der Regel nur auf einem Chromosom tragen.
Bei einer autosomal-dominanten Vererbung ist bereits das Vorhandensein eines defekten Gens für den Ausbruch der Erkrankung ausreichend. Falls es sich nicht um eine spontane Neumutation handelt, ist eines der beiden Elternteile auch von dieser Erkrankung betroffen. In dem Fall gibt die erkrankte Person die Krankheit in 50 Prozent der Fälle auch an das Kind weiter.
Bei einigen Stoffwechselerkrankungen spielen neben genetischen Faktoren auch gewisse Risikofaktoren eine Rolle. Diese beeinflussen die Wahrscheinlichkeit, dass die Krankheit auftritt und behandlungsbedürftig wird. Die klassischen Risikofaktoren für Stoffwechselerkrankungen sind eine unausgewogene Ernährung, ein Mangel an Bewegung und Übergewicht. Zudem erhöhen auch Alkohol und Rauchen das Erkrankungsrisiko.
Seltene angeborene Stoffwechselerkrankungen
Die seltenen angeborenen Stoffwechselerkrankungen sind meist nur spezialisierten Ärzten sowie den Betroffenen und ihren Angehörigen bekannt. Um einen Einblick in die Folgen eines gestörten Stoffwechsels zu geben, werden vier Erkrankungen beispielhaft vorgestellt. Sie zeigen, die Vielfalt der Symptome und welche weitreichenden Auswirkungen der Ausfall bereits eines einzigen Enzyms haben kann.
Morbus Wilson
Bei Morbus Wilson handelt es sich um eine seltene Erkrankung des Kupferstoffwechsels. Da überschüssiges Kupfer nicht ausgeschieden werden kann und sich stattdessen in Organen ansammelt, wird die Erkrankung auch als Kupferspeicherkrankheit bezeichnet.
Schätzungen zufolge sind etwa 30 Menschen pro 1 Million Einwohner betroffen. In der Mehrzahl der Fälle tritt Morbus Wilson erstmals im Alter zwischen fünf und 45 Jahren auf, Personen weiblichen und männlichen Geschlechts sind gleichermaßen betroffen.
Der menschliche Körper benötigt Kupfer für zahlreiche Enzym-Funktionen. Das Spurenelement wird über die Nahrung aufgenommen, im Dünndarm resorbiert und in die Leber transportiert. Reguliert wird die Verwertung und Ausscheidung durch das Kupfer-Transportprotein ATP7B. Bei Menschen mit Morbus Wilson ist die Aktivität des Proteins in den Leberzellen infolge eines Gen-Defekts beeinträchtigt oder nicht vorhanden. Überschüssiges Kupfer wird deshalb nicht oder allenfalls in zu geringem Umfang über die Galle ausgeschieden, sondern lagert sich in der Leber und mit Fortschreiten der Erkrankung in weiteren Organen, z.B. Gehirn und Augen, ab.
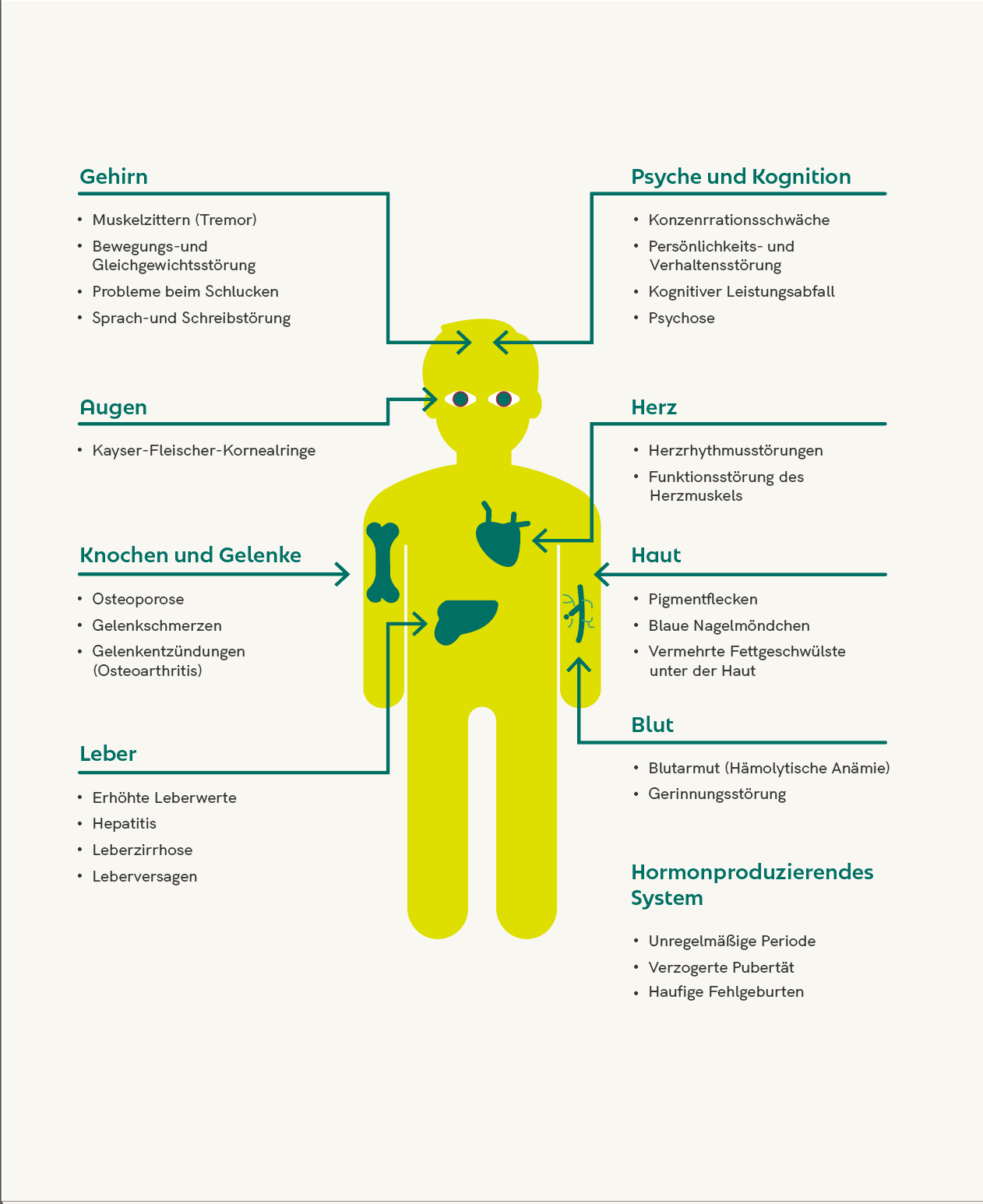
Wie untenstehende Grafik zeigt, kann sich die Kupferspeicherkrankheit durch zahlreiche Symptome ganz unterschiedlicher Art bemerkbar machen. Um welche Symptome es sich handelt, hängt davon ab, in welchen Geweben sich das Kupfer angesammelt hat.
Bei einem Auftreten im Kindesalter manifestieren sich vorwiegend hepatische Symptome, gegebenenfalls zeigen sich auch Symptome neurologischer Art. Tritt die Erkrankung erstmals bei Jugendlichen nach der Pubertät oder Erwachsenen in Erscheinung, sind häufig neben der Leber Gehirn und Psyche betroffen.
Ein typisches Merkmal der Erkrankung kann durch eine Spaltlampenuntersuchung an den Augen festgestellt werden. Durch die Kupfer-Ansammlung entstehen rund um die Iris grünlich-goldene Ringe. Das als Kayser-Fleischer-Ringe bezeichnete Phänomen wird bei der Mehrzahl der Betroffenen mit neurologischen Symptomen beobachtet sowie bei jedem zweiten Patienten ohne neurologische Beschwerden.
AL-Amyloidose
Unter Amyloidose fasst man Erkrankungen zusammen, die auf einer Proteinfehlfaltung beruhen. Dadurch sammeln sich in verschiedenen Geweben Amyloidproteine an, die zu schweren Organschädigungen führen können. Die häufigste Form ist die Leichtketten-Amyloidose, auch primäre oder AL-Amyloidose genannt. Spezielle Zellen im Knochenmark, sogenannte Plasmazellen, vermehren sich dabei stark und produzieren strukturell fehlerhafte Leichtketten. Diese werden ins Blut abgegeben und lagern sich dann in den Organen ab.
Die Erkrankung ist zu 90 bis 95 Prozent erworben und nicht angeboren. Sie wird vor allem bei Personen im mittleren oder fortgeschrittenen Alter diagnostiziert, Männer sind von der Amyloidose der Leichtketten häufiger als Frauen betroffen.
Aufgrund der abnormen Faltung sind die Proteine nicht abbaubar, sondern verklumpen und bilden sogenannte Amyloidfibrillen – straffe, lineare Fasern, die sich in verschiedenen Organen und Geweben ablagern können.
Zu den Risikofaktoren für die Entwicklung der AL-Amyloidose zählen chronische Entzündungserkrankungen und Nierenerkrankungen, einschließlich einer dialysepflichtigen Niereninsuffizienz.
Die Symptomatik ist abhängig von den betroffenen Organsystemen. Bei etwa 74 Prozent der Patienten ist das Herz betroffen, in ca. 65 Prozent der Fälle kommt es zu Amyloid-Ablagerungen in den Nieren.
Die Erkrankung äußert sich anfänglich meist mit unspezifischen Beschwerden wie Müdigkeit und einer geringeren körperlichen Belastbarkeit, Inappetenz und Gewichtsabnahme. Das Auftreten organbezogener Symptome deutet auf ein fortgeschrittenes Krankheitsstadium infolge massiver Amyloid-Ablagerungen in den entsprechenden Organen hin. Eine Schädigung des Herzens kann sich durch Herzrhythmusstörungen, Kurzatmigkeit oder Wassereinlagerungen in Beinen und Rippenfell bemerkbar machen. Proteinurie (vermehrte Ausscheidung von Eiweißen), schäumender Urin, Wasseransammlungen im Gewebe, Kreislaufschwäche und niedriger Blutdruck können Anzeichen für eine Nierenbeteiligung sein. Kribbeln, Taubheit und Schwellungen in Zehen oder Fingern, stechende Schmerzen oder ein Schwindelgefühl beim Aufstehen weisen darauf hin, dass das Nervensystem betroffen ist. Bei Amyloid-Ablagerungen im Magen-Darm-Trakt kann es aufgrund einer beeinträchtigten Resorptionsfähigkeit des Darms zu einem Nährstoffmangel und beträchtlichem Gewichtsverlust kommen.
Einer frühen Diagnosestellung kommt bei der AL-Amyloidose eine entscheidende Bedeutung zu, da die Erkrankung zu lebensbedrohlichen Komplikationen führen kann.
Ein typisches Merkmal der Erkrankung kann durch eine Spaltlampenuntersuchung an den Augen festgestellt werden. Durch die Kupfer-Ansammlung entstehen rund um die Iris grünlich-goldene Ringe. Das als Kayser-Fleischer-Ringe bezeichnete Phänomen wird bei der Mehrzahl der Betroffenen mit neurologischen Symptomen beobachtet sowie bei jedem zweiten Patienten ohne neurologische Beschwerden.
Hypophosphatasie (HPP)
Die Hypophosphatasie, kurz HPP genannt, ist eine seltene Erkrankung des Knochenstoffwechsels, die die Mineralisation des Knochens, die wiederum zur Bildung gesunder Knochen notwendig ist, beeinträchtigt und sich zudem auf weitere Organe auswirken kann. Die Erbkrankheit kann sich in jedem Lebensalter manifestieren. Die Prävalenz (Krankheitshäufigkeit) variiert in Abhängigkeit vom Verlaufstyp stark und reicht von 1:6.370 bis 1:300.000. Aufgrund der teils unspezifischen Symptome, die auch auf andere Erkrankungen zutreffen können, wird die Diagnose HPP oft erst spät gestellt.
Wie bereits beschrieben, ist zur Bildung stabiler Knochen die ausreichende Versorgung mit Kalzium und Phosphat erforderlich. Für den Einbau der Mineralstoffe in die Knochen sorgt das Enzym alkalische Phosphatase (AP). Bei HPP-Patienten wird das Enzym aufgrund einer Genmutation jedoch in zu geringer Konzentration im Körper gebildet und/oder zeigt zu wenig Aktivität, dadurch werden die Knochen nicht ausreichend mineralisiert, sind weich und instabil. Lagern sich Kalzium und Phosphat stattdessen in Muskeln, Gelenken und anderen Organen ab, kann das starke Muskel- und Gelenkschmerzen sowie schwere Organschäden hervorrufen.
Je nachdem, wann sich die Hypophosphatasie erstmals bemerkbar macht, unterscheidet man in der Medizin sechs Formen der Erkrankung. Die schwersten Formen sind die perinatale und infantile HPP, die sich bereits im Mutterleib oder kurz nach der Geburt zeigen (erste Symptome innerhalb von sechs Monaten) und aufgrund schwerer Mineralisationsstörungen häufig zum Tod durch Versagen der Atmung führen. Die weiteren Formen, die im Kindes- oder Erwachsenenalter in Erscheinung treten, sind durch eine komplexe Symptomatik gekennzeichnet.
Aufgrund der schwachen, spröden Knochen kommt es häufig zu schlecht verheilenden Brüchen und einer Verformung der Beinknochen. Kinder und Erwachsene sind oftmals von einem vorzeitigen Zahnverlust betroffen. Zudem kann sich HPP durch Knochen- und Muskelschmerzen, Muskelschwäche, Gelenkentzündungen und gichtähnliche Beschwerden äußern, nahezu ein Drittel der Betroffenen benötigt eine Gehhilfe. Kalziumablagerungen in den Nieren können die Nierenfunktion beeinträchtigen und im schlimmsten Fall ein Nierenversagen verursachen. Die Erkrankung kann zusätzlich mit Magen-Darm-Beschwerden wie Übelkeit und Verdauungsproblemen einhergehen sowie mit unspezifischen Symptomen wie starker Erschöpfung und mangelnder Konzentrationsfähigkeit.

Lysosomale saure Lipase-Defizienz
Bei der lysosomalen sauren Lipase-Defizienz, kurz LAL-D, handelt es sich um eine seltene, lebensbedrohliche Stoffwechselerkrankung.

Hypophosphatasie
Die Hypophosphatasie ist eine erblich bedingte Stoffwechselerkrankung, die sich auf Knochen, Zähne, Muskulatur und weitere
Lysosomale saure Lipase-Defizienz (LAL-D)
Die lysosomale saure Lipase-Defizienz beruht auf einer seltenen Störung des Fettstoffwechsels im Lysosom. Bei betroffenen Patienten besteht ein Mangel am für den Abbau von Lipiden notwendigen Enzym lysosomale saure Lipase (LAL). Die Zellen können durch die Abbaustörung zu wenig freies Cholesterin und freie Fettsäuren produzieren. Die nicht abgebauten Fette sammeln sich stattdessen in lebenswichtigen Organen an und können schwerwiegende Schädigungen verursachen.
LAL-D kann Menschen in jedem Lebensalter betreffen, auch bereits Säuglinge. Die Symptome und Folgen der lysosomale saure Lipase-Defizienz hängen davon ab, wie hoch die Restaktivität der LAL-Enzyms ist.
Die schwere Verlaufsform, die sich häufig bereits in den ersten Lebenstagen manifestiert und durch ein vollständiges Fehlen des LAL-Enzyms gekennzeichnet ist, wird bisweilen nach ihrem Entdecker, dem israelischen Arzt Moshe Wolman, auch Morbus Wolman genannt. Typisch für die Erkrankung von Säuglingen sind anhaltendes Erbrechen und schwerer Durchfall sowie stark vergrößerte Leber und Milz. Infolge der beeinträchtigten Versorgung mit wichtigen Nährstoffen kommt es zu einem langsameren Wachstum und einer verzögerten Entwicklung der Kinder. Die Erkrankung schreitet schnell voran, kann lebensbedrohliche Ausmaße annehmen und zu einem Leberversagen führen.
Ist eine verminderte Enzym-Aktivität vorhanden, tritt die Erkrankung im Kindes- und Erwachsenenalter in Erscheinung. Bei knapp 90 Prozent der betroffenen Personen werden erste Krankheitszeichen bis zum 12. Lebensjahr festgestellt.
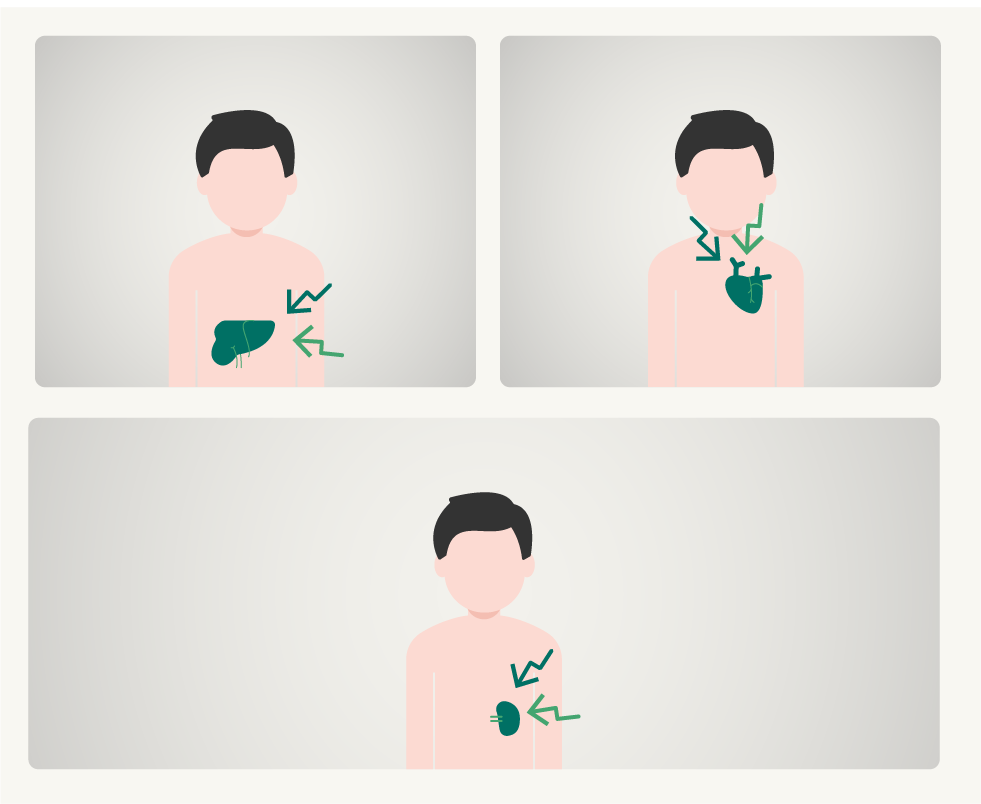
Bei einem späteren Auftreten kann sich die lysosomale saure Lipase-Defizienz je nach Patient mit unterschiedlichen, teilweise unspezifischen, Symptomen bemerkbar machen. In 87 Prozent der Fälle sind mehrere Organe betroffen, am häufigsten die Leber. Neben einer Vergrößerung der Leber werden oftmals narbige Veränderungen (Leberfibrose) beobachtet, aus denen sich eine Leberzirrhose entwickeln kann. Zudem zeigen sich erhöhte Blutfettwerte
(chronische Hyperlipidämie), atherosklerotische Veränderungen an Arterien und eine vergrößerte Milz.
Diagnose: Stoffwechselerkrankungen erkennen
Dank der Fortschritte in der Medizin und Forschung können heute Stoffwechselstörungen schneller erkannt werden. Dies ist bei vielen Erkrankungen entscheidend wichtig, da eine frühzeitige Behandlung spätere Folgeschäden verhindern oder zumindest begrenzen kann. Eine erste Untersuchung auf 14 angeborene Stoffwechsel- und Hormonstörungen findet in Deutschland standardmäßig bereits in den ersten Lebenstagen im Rahmen des Neugeborenen-Screenings statt. Ziel ist die frühzeitige Erkennung von Stoffwechselerkrankungen, die unbehandelt oder bei zu spätem Behandlungsbeginn zu schweren Schäden führen.
Während dieses Screening durchgeführt wird, ohne dass zum Untersuchungszeitpunkt Symptome zu beobachten sind, wird im weiteren Leben erst nach Stoffwechselstörungen gesucht, wenn die Betroffenen mit Beschwerden einen Arzt aufsuchen. Erste Hinweise auf die Krankheitsursache liefert die Anamnese, bei der der Betroffene seine Symptome schildert. Blut- und Urinuntersuchungen tragen zur Diagnosestellung bei. Dank der modernen Analytik können die Blutwerte von Stoffwechselprodukten gemessen werden, ebenso der Spiegel von Hormonen und die Aktivität einzelner Enzyme. Hinzu kommen ergänzende Untersuchungen wie z.B. der Ultraschall der inneren Organe sowie je nach Symptombild weiterführende Tests, wie z.B. eine Knochendichtemessung. In einigen Fällen ist auch eine genetische Untersuchung hilfreich, um Gendefekte zu erkennen. Der behandelnde Arzt stellt die Diagnose unter Berücksichtigung aller Untersuchungsergebnisse. Bei häufig auftretenden Stoffwechselerkrankungen wie dem Diabetes mellitus (Zuckerkrankheit) ist die Diagnosestellung relativ einfach. In Anbetracht der großen Anzahl an seltenen Stoffwechselerkrankungen und den teils unspezifischen Symptomen dauert es dagegen bei seltenen Erkrankungen häufig länger, bis die korrekte Diagnose gestellt wird.
Ein bis zwei Personen pro tausend Einwohner sind von einer angeborenen Stoffwechselerkrankung betroffen. Dabei zeigen sich in 80% der Fälle bereits Symptome in Kindesalter. Kinderärzte sind daher bei der Erkennung der Stoffwechselerkrankungen besonders gefordert.
Wenn Symptome der seltenen Stoffwechselerkrankungen erst später auftreten, sind sie häufig unspezifisch und stellen hohe Anforderungen an die Differenzialdiagnostik. Auf die Problematik von Fehldiagnosen oder einer teilweise jahrelangen Dauer bis zur korrekten Diagnosestellung weisen z.B. Aktionen der Patientenorganisation Hypophosphatasie Deutschland e.V. hin. Gemeinsam mit dem Biotech-Unternehmen Alexion, einem Pionier in der Erforschung seltener Erkrankungen und der Entwicklung innovativer Medikamente, ist die Initiative „Sieht aus wie… Ist aber HPP“ entstanden. Auf Schaubildern und Videos wird der Leidensweg von Patienten skizziert, um die Öffentlichkeit darauf aufmerksam zu machen, welche Herausforderung das Leben mit einer seltenen Erkrankung darstellt.
Behandlung: Zielgerichtete Therapieansätze
Die konkrete Behandlungsstrategie ist abhängig von der vorliegenden Stoffwechselstörung und den dadurch ausgelösten Beschwerden. Neben der Therapie der akut vorhandenen Symptome ist gerade bei Stoffwechselerkrankungen die Vermeidung von Krankheitsprogression und Langzeitschäden entscheidend. Zum Teil kann das fehlende oder in nicht ausreichender Konzentration vorhandene Enzym dem Körper durch eine Enzymersatztherapie zur Verfügung gestellt werden. Bei anderen Therapieansätzen wird die Ausscheidung von schädigenden Abfallstoffen gefördert. Liegt ein Mangel an bestimmten Stoffwechselprodukten vor, können diese gezielt zugeführt werden.
Da bei etlichen Stoffwechselerkrankungen die Verwertung bestimmter Nahrungsbestandteile beeinträchtigt ist, kann das Krankheitsgeschehen mithilfe einer auf die individuellen Bedürfnisse zugeschnittenen Ernährungstherapie positiv beeinflusst werden.
Steht der Verdacht auf das Vorliegen einer seltenen Stoffwechselerkrankung im Raum, ist der Besuch eines spezialisierten Zentrums für Stoffwechselerkrankungen anzuraten. Die dort praktizierenden Ärzte weisen eine hohe Expertise für dieses Spezialgebiet auf und können die Stoffwechselstörung differenzialdiagnostisch abklären und beurteilen. Bei der individuellen Therapieplanung greifen sie auf die Erfahrungen in der Therapie von seltenen Erkrankungen zurück und können Behandlungsoptionen anbieten, die auf dem aktuellen Stand der Forschung beruhen.
Glossar
| AL-Amyloidose | Leichtketten-Amyloidose, seltene Proteinablagerungskrankheit des Bluts mit Auswirkungen auf multiple Organe |
| Alkalische Phosphatase (AP) | Enzym zur Hydrolysierung von Phosphorsäureestern |
| Aminosäuren | Bilden die Bausteine von Eiweißen |
| Amyloidfibrillen | Fehlgefaltete Eiweiße mit faserartiger Struktur |
| atherosklerotisch | Krankhafte Veränderung der Gefäßwände |
| ATP7B | Spezialisiertes Eiweiß für den Transport von Kupfer im Blut |
| autosomal-dominant | Erbgang, Auftreten der Erkrankung schon beim Gendefekt auf einem der beiden Chromosomen |
| autosomal-rezessiv | Erbgang, Auftreten der Erkrankung nur, wenn eine Gendefekt auf beiden Chromosomen parallel auftritt |
| Diabetes mellitus | Zuckerkrankheit |
| Enzym | Fördert chemische Reaktionen im Körper |
| Enzymersatztherapie | Zufuhr von synthetischen Enzymen zum Ausgleich eines Enzymmangels |
| Gendefekt | Veränderung des Erbgutes mit nachteiliger Auswirkung auf den Körper |
| Glykogen | Speicherform der Glukose |
| Glykolyse | Stoffwechselweg zum Abbau von Glukose |
| HPP | Hypophosphatasie, seltene Erkrankung des Knochenstoffwechsels |
| Hyperlipidämie | Zu hoher Blutfettspiegel |
| Hypophyse | Hirnanhangsdrüse, eine Hormondrüse im Kopf |
| Kayser-Fleischer-Ringe | Charakteristische Kupferablagerungen in der Hornhaut des Auges |
| LAL-D | Lysosomale saure Lipase-Defizienz, seltene Erkrankung des Fettstoffwechsels |
| Lipide | Fette |
| Lipoproteine | Transportvehikel im Blut, bestehend aus Eiweißen und Fetten |
| Morbus Wilson | Kupferspeicherkrankheit, seltene Erkrankung des Kupferstoffwechsel |
| Neumutation | Erstmaliges und spontanes Auftreten einer Genveränderung im Erbgut |
| Niereninsuffizienz | Mangelnde Funktionalität der Niere |
| Osteoblasten | Knochenbildende Zellen |
| Osteoklasten | Knochenabbauende Zellen |
| perinatal | Kurz vor oder während der Geburt eintretend |
| Protein | Eiweiß |
| Proteinurie | Übermäßige Ausscheidung von Eiweiß über die Niere |
| Proteolyse | Stoffwechselweg zum Abbau von Eiweißen |
Quellen
Bernstein, Donna L., Helena Hülkova, Martin G. Bialer, und Robert J. Desnick. 2013. „Cholesteryl Ester Storage Disease: Review of the Findings in 135 Reported Patients with an Underdiagnosed Disease“. Journal of Hepatology 58 (6): 1230–43.
Burton, Barbara K., Patrick B. Deegan, Gregory M. Enns, Ornella Guardamagna, Simon Horslen, Gerard K. Hovingh, Steve J. Lobritto, u. a. 2015. „Clinical Features of Lysosomal Acid Lipase Deficiency“. Journal of Pediatric Gastroenterology & Nutrition 61 (6): 619–25.
Capone, Kristin, und Ruba K. Azzam. 2018. „Wilson’s Disease: A Review for the General Pediatrician“. Pediatric Annals 47 (11).
Tomasz Litwin, Petr Dusek, Peter Ferenci, Svetlana Lutsenko, Valentina Medici, Janusz K. Rybakowski, Karl Heinz Weiss, and Michael L. Schilsky. 2018. “ Wilson Disease ”. Nature Reviews. Disease Primers 4 (1): 21.
Dispenzieri, Angela, and Giampaolo Merlini. 2016. “ Immunoglobulin Light Chain Systemic Amyloidosis ”. In Plasma Cell Dyscrasias, edited by Aldo M. Roccaro and Irene M. Ghobrial, 169:273-318. Cancer Treatment and Research. Cham: Springer International Publishing.
Donner, M, A Erhardt, and D Häussinger. 2010. “ Metabolic diseases of the liver ”. DMW – German Medical Weekly 135 (50): 2540-47.
European Association for Study of Liver. 2012. „EASL Clinical Practice Guidelines: Wilson’s Disease“. Journal of Hepatology 56 (3): 671–85.
Gertz, Morie A. 2020. „Immunoglobulin Light Chain Amyloidosis: 2020 Update on Diagnosis, Prognosis, and Treatment“. American Journal of Hematology 95 (7): 848–60.
Hase, Claudia. 2006. “ Enzyme Replacement Therapy in Congenital Metabolic Disorders ”. Pediatric and Adolescent Medicine 6 (04): 241–47.
Ihne, Sandra, Caroline Morbach, Claudia Sommer, Andreas Geier, Stefan Knop, and Stefan Störk. 2020. “ Amyloidosis—the Diagnosis and Treatment of an Underdiagnosed Disease ”. German Medical Journal Online, March.
Jandl, Nico Maximilian, Alexander Volk, and Florian Barvencik. 2019. “ Hypophosphatasia – A clinically and genetically variable disease ”. Medical Genetics 31(4):364–71.
Karakostas, P., Dolscheid-Pommerich, R., Hass, M.D. et al. Prävalenz der Hypophosphatasie bei adulten Patienten in der Rheumatologie. Z Rheumatol (2021).
Konstantopoulou, Vassiliki. 2021. „Angeborene Stoffwechselerkrankungen – Orphan Diseases aus der Sicht der Pädiatrie: Empfohlene Strategien zur Minimierung einer Diagnoseodyssee“. Journal für Klinische Endokrinologie und Stoffwechsel 14 (4): 134–39.
Lalioti, Vassiliki, Ignacio Sandoval, Doris Cassio, und Jean-Charles Duclos-Vallée. 2010. „Molecular Pathology of Wilson’s Disease: A Brief“. Journal of Hepatology 53 (6): 1151–53.
On behalf of the Rare Bone Disease Action Group of the European Calcified Tissue Society, M. L. Bianchi, N. J. Bishop, N. Guañabens, C. Hofmann, F. Jakob, C. Roux, und M. C. Zillikens. 2020. „Hypophosphatasia in Adolescents and Adults: Overview of Diagnosis and Treatment“. Osteoporosis International 31 (8): 1445–60.
Reiner, Željko, Ornella Guardamagna, Devaki Nair, Handrean Soran, Kees Hovingh, Stefano Bertolini, Simon Jones, u. a. 2014. „Lysosomal Acid Lipase Deficiency – An under-Recognized Cause of Dyslipidaemia and Liver Dysfunction“. Atherosclerosis 235 (1): 21–30.
van de Loo I, Harbeck B (2020) Rare Metabolic Disorders. In: Specialist knowledge in endocrinology and diabetology. Springer, Berlin, Heidelberg.
Whyte, Michael P. 2016. „Hypophosphatasia — Aetiology, Nosology, Pathogenesis, Diagnosis and Treatment“. Nature Reviews Endocrinology 12 (4): 233–46.
Zschocke, Johannes. 2015. “Hereditary Metabolic Diseases – A Review”. Medical Genetics 27(3):268–75.
Zufrieden?
Du hast die Informationen erhalten, nach denen du gesucht hast? Das freut uns. Wir arbeiten täglich mit viel Enthusiasmus und Herzblut daran, medizinische Fragen ausführlich, verständlich und korrekt zu beantworten. Lass uns ein Like da. So wissen wir, dass unsere Inhalte ankommen.
Bildnachweis: istockphoto.com | fizkes





